تست اندوتوکسین یا bacterial endotoxin test که به آن BET نیز گفته میشود روشی آزمایشگاهی است که در آن میزان اندوتوکسین در نمونه بیولوژیک یا در سطوح مورد ارزیابی قرار میگیرد. تست LAL که مخفف کلمه Limulus Amebocyte Lysate است یکی از معروف ترین تست ها برای اندازه گیری مقدار اندوتوکسین باکتریایی در نمونه های مختلف در فرایندهای تحقیقاتی و تولیدی است. اصول تست LAL بر مبنای کواگولاسیون ای است که در مایع خارج سلولی یا همولنف خرچنگ نعل اسبی در حضور لیپوپلی ساکارید اتفاق می افتد. در ادامه با تست سنجش میزان اندوتوکسین به روش LAL آشنا خواهیم شد.
اصول روش LAL
همانطور که گفته شد، اولین اصل روش LAL، کواگولاسیون همولنف خرچنگ نعل اسبی است که ناشی از زنجیره ای واکنش های شیمیایی است که در نهایت موجب ایجاد لخته میشوند. برای فعال سازی این زنجیره واکنش ها بایستی سرین پروتئاز هایی که در همولنف به صورت پروآنزیم هستند فعال شوند تا بتوانند زنجیره کواگولاسیون را فعال کنند. نکته جالب توجه اینجاست که این سرین پروتئازها با حضور کمترین میزان از لیپوپلی ساکارید ( LPS ) باکتریایی فعال میشوند. نکته جالب اینجاست که میزان LPS ای که میتواند سرین پروتئازهای خرچنگ را فعال کند در حد پیکوگرم است.
به علت اینکه بخش زیادی از اجزای زنجیره کواگولاسیون به واسطه گرانول های ریزی در همولنف خرچنگ به نام amebocytes انجام میشود، به همین دلیل این روش به روش Limulus Amebocyte Lysate نام گذاری شده است. در روش LAL فرایند ایجاد ژل به عنوان یک سیگنال برای حضور اندوتوکسین در نمونه است و این روش به دو صورت کمی و کیفی قابل انجام است. لازم به ذکر است، بر خلاف بسیاری از روش های آزمایشگاهی که موجود آزمایشگاهی پس از آزمایش آسیب دیده یا از بین خواهد رفت، در روش LAL و در فرایند استخراج همولنف خرچنگ اسب آبی، خرچنگ آسیبی ندیده و بخشی از همولنف خرچنگ استخراج شده و خرچنگ به محل زندگی خود انتقال داده خواهد شد.
مکانیسم روش سنجش اندوتوکسین با LAL
همانطور که گفته شد، رویدادی که در همولنف خرچنگ نعل اسبی رخ میدهد، حاصل فعال شدن چرخه پروتئازی است که در نهایت منجر به ایجاد لخته میشود. LPS پروآنزیم فاکتور C را به صورت اتوکاتالیک فعال کرده و آن را به فاکتور C فعال تبدیل میکند. فاکتور C، فاکتور B را فعال میکند و فاکتور B، پروآنزیم ایجاد کننده ژل یا لخته را به آنزیم فعال تبدیل میکند. فاکتور لخته کننده دو جزء محلول لخته را به یکدیگر متصل میکند و به این ترتیب یک جزء نامحلول ایجاد کرده که حاصل آن تشکیل حالت ژل خواهد شد. ترکیب ایجاد شده از نظر ساختاری شباهت زیادی به فیبرینوژن در خانواده بند پایان است.
زنجیره کواگولاسیون علاوه بر فرایند گفته شده با β-D-glucan و از طریق فعال شدن فاکتور G که آن هم یک سرین پروتئاز است هم میتواند موجب ایجاد ژل شود. به همین دلیل β-D-glucan یکی از عوامل مداخله کننده در فرایند تست LAL بوده و به همین دلیل در هنگام انجام تست بایستی از ترکیبات مهار کننده β-D-glucan نیز بایستی استفاده شود.
تست LAL در ابتدا یک تست کاملا کیفی بود و صرفا وجود یا عدم وجود اندوتوکسین به واسطه این تست بررسی میشد اما با توسعه روند انجام تست LAL امروزه این تست به یک تست کاملا کمی تبدیل شده و با استفاده از کیت های LAL میزان دقیق اندوتوکسین به صورت دقیق مشخص میشود.
انواع تست LAL:
همانطور که گفته شد روش LAL سنتی روشی کیفی بوده و به جهت کمی سازی تست تغییراتی در تست اصلی داده شده تا بتوانیم نتایجی دقیق از میزان اندوتوکسین موجود در نمونه به دست بیاوریم.
سه روش اصلی سنجش اندوتوکسین که بر مبنای روش LAL توسعه یافته اند عبارتند از:
روش ژل کلات ( Chromogenic method )
روش کروموژنیک ( Chromogenic method )
روش کدورت سنجی ( Turbidimetric method )
سنجش اندوتوکسین به روش ژل کلات ( Gel-clot method )
روش gel-clot یکی از ساده ترین انواع روش های تست LAL و در واقع همان روش سنتی ایجاد لخته است و میتواند حضور یا عدم حضور اندوتوکسین را در نمونه مشخص کند. همانطور که گفته شده در روش سنتی وقتی اندوتوکسین با LAL مواجه میشود بر اثر فعالیت زنجیره آنزیمی پروتئازی amoebocyte coagulogen موجود در LAL تبدیل به لخته یا ژل میشود. در کیت های تجاری مبتنی بر Gel-Clot تغییر ویژه ای در روش انجام تست داده نشده و تنها با ایجاد رقت سریالی از ماده مورد آزمایش و بررسی ایجاد لخته در زمان مشخص شده در پروتکل کیت، حدود میزان اندوتوکسین موجود در نمونه مشخص میشود.
روش gel-clot به نظر حساس ترین و دقیق ترین نوع تست LAL بوده و کمترین میزان مثبت کاذب نسبت به سایر روش ها در این روش مشاهده شده است. همچنین این روش در فارماکوپه آمریکا، اروپا و ژاپن به عنوان روش استاندارد برای تعیین وجود اندوتوکسین در نمونه دارویی معرفی گردیده است. با این وجود این روش زمان بر بوده و قابلیت انجام اتوماتیک ندارد به همین دلیل در حجم های بالای نمونه و امکان ایجاد خطای انسانی این روش توصیه نمیشود.
سنجش اندوتوکسین به روش کروموژنیک ( Chromogenic method ) :
روش کروموژنیک برای اولین بار در سال 1977 معرفی شد. در این روش سوبسترای رنگ زا ( کروموژن ) ای با توالی آمینو اسیدی مشابه محل برش کواگلوژن به محیط واکنش اضافه میشود. LAL فعال شده توسط اندوتوکسین این توالی آمینو اسیدی را برش داده و باعث میشود که کروموفور pNA (p-nitroanilide) آزاد شده و در محیط رنگ زرد ایجاد شود.
مولکول pNA در طول موج مشخصی جذب کرده و در روش کروموژنیک میزان جذب نوری را در این طول موج اندازه گیری میکنند. میزان جذب نوری به صورت مستقیم مشخص کننده میزان اندوتوکسین موجود در نمونه است. میزان جذب میتواند به صورت مستمر در طول فرایند واکنش صورت گیرد و یا تنها در پایان واکنش اندازه گیری شود.
تست اندوتوکسین کروموژنیک Kinetic و end-point
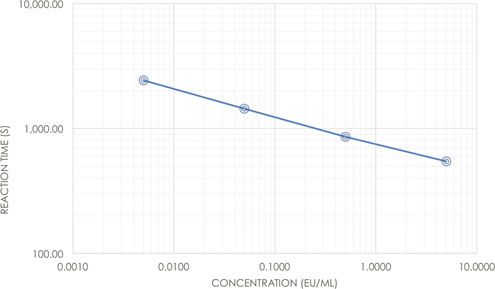
در روش Kinetic میزان اندوتوکسین بر اساس زمان واکنش نسبت به زمان واکنش در منحنی استاندارد غلظت اندوتوکسین محاسبه میشود.
در روش end-point-chromogenic خوانش نتیجه پس از مدت مشخصی از انکوباسیون اندازه گیری شده و میزان جذب در زمان مشخص ملاک اندازه گیری غلظت اندوتوکسین در نمونه خواهد بود.
سنجش اندوتوکسین به روش کدورت سنجی ( Turbidimetric method )
در روش کدورت سنجی، میزان کدورت ایجاد شده در اثر واکنش LAL با اندوتوکسین اندازه گیری شده و برای تعیین میزان اندوتوکسین استفاده میشود. روش کدورت سنجی روش تغییر یافته از gel-clot است که قابلیت انجام اتوماتیک را دارا است. در این روش ترکیب LAL تغییر یافته ای استفاده میشود که مقدار کمتری از کواگلوژن نسبت به حالت عادی داشته و به همین دلیل به جای ایجاد لخته، در ماده ایجاد کدورت میکند. مزیت روش کدورت سنجی این است که یک روش کاملا کمی بوده و به دقت میتواند میزان اندوتوکسین را اندازه گیری نماید.
در سنجش اندوتوکسین به روش کدورت سنجی، میزان مشخصی از نمونه و محلول LAL در دمای 37 درجه انکوبه شده و میزان کدورت ایجاد شده نسبت به منحنی استاندارد ارزیابی خواهد شد. این روش نیز مشابه روش رنگ سنجی، می تواند به صورت ادامه دار ( سنجش کدورت به صورت پیوسته در کل زمان انکوباسیون ) و یا به صورت سنجش در پایان زمان انکوباسیون انجام شود.
از معایب روش کدورت سنجی این است که انجام این روش برای ترکیباتی که خود کدورت یا رنگ دارند دشوار یا امکان ناپذیر است.
انتخاب بهترین روش سنجش اندوتوکسین:
هر سه روش ذکر شده در این نوشته توسط فارماکوپه های معتبر اروپا، آمریکا، انگلیس و ژاپن مورد تایید بوده و از نظر سازمان غذا و داروی ایران تا تاریخ نگارش این مطلب، هر سه روش قابل قبول هستند. البته ممکن است برای دارو یا شرایط خاصی نیاز به روش مشخصی باشد که بسته به درخواست شما و استعلام های انجام شده از سازمان و مرور مطالب موجود در فارماکوپه روش بهینه برای درخواست شما اجرا خواهد شد. در آرک زیست آزما انجام تمامی روش های سنجش اندوتوکسین امکان پذیر است.
تست اندوتوکسین در سطوح
برای سنجش اندوتوکسین در دستگاه ها، سطوح یا ویال های مورد استفاده در فرایند دارویی، بایستی سطوح با استفاده از آب عاری از اندوتوکسین تیمار شده و پس از آن نمونه آب جهت ارزیابی وجود اندوتوکسین مورد استفاده قرار گیرد.
این میزان بسته به دستگاه مورد نظر متفاوت است، اما بایستی حداقل میزان آبی باشد که بتواند کلیه سطوح مورد آزمایش را پوشش دهد. برای ارزیابی آلودگی اندوتوکسین در مسیرهای آبی و لوله ها بایستی آب با دمای 37 درجه از این مسیرها عبور داده شود. البته مدت زمان تماس آب با سیستم نباید کمتر از 1 ساعت باشد. دستگاه یا ابزارهایی که کوچک بوده و قابلیت معلق شدن در آب را دارا هستند، بایستی به مدت بیشتر از 60 دقیقه در آب با دمای 37 تا 40 درجه روی شیکر غوطه ور شوند.
استفاده از آب نامناسب و یا نمونه گیر اشتباه در این زمینه میتواند موجب جواب مثبت کاذب و یا منفی کاذب در آزمون اندوتوکسین گردد. لازم به ذکر است که شرایط عنوان شده، شرایط عمومی نمونه گیری LAL است و ممکن است شرایط نمونه گیری بسته به نوع دستگاه و شرایط مورد نظر متفاوت باشد.
پرورش خرچنگ نعل اسبی:
خرچنگ نعلاسبی (Horseshoe crab) که به فسیل زنده نیز مشهور است یکی از گونه های در حال انقراض است. خون این خرچنگ به علت وجود هموسیانین ( به جای هموگلوبین ) و وجود ترکیبات مس در هموسیانین، به رنگ آبی است. در خون خرچنگ نعل اسبی آمبوسیت ها نقش ایمنی زایی داشته و همین آمبوسیت ها در جنس L.polyphemus هستند که برای تولید ترکیب LAL مورد استفاده قرار میگیرند.

اگرچه در اوایل شناسایی تاثیر شگفت انگیز LAL باعث شده بود که نسل این خرچنگ ها به خطر بیفتد، اما فراگیر شدن استفاده از LAL کم کم باعث شد که توجه بیشتری به خرچنگ نعل اسبی صورت گرفته و امروزه فارم های مصنوعی زیادی جهت پرورش، تکثیر و نگهداری از خرچنگ نعل اسبی ایجاد شده است. این فارم ها خرچنگ را پرورش داده و از خرچنگ به اندازه ای خون استخراج میکنند که تهدیدی برای سلامت موجود نبوده و مجدد آن را به فارم باز میگردانند.

تجارت پر سود LAL باعث شده امروزه شرکت های بزرگی به تولید کیت و مواد اولیه برای سنجش اندوتوکسین اقدام کنند و مراکز بزرگ پرورش خرچنگ نعل اسبی در سراسر جهان ایجاد شود. امروزه شرکت های بزرگی در دنیا تولید کننده ترکیبات مرتبط با اندوتوکسین هستند که پر استفاده ترین کیت اندوتوکسین در ایران کیت های لونزا، اندوسیف و بیواندو هستند. کیت اندوتوکسین لونزا ، ساخت شرکت سوئیسی و معروف لونزا ، کیت اندوتوکسین ENDOSAFE ساخت شرکت آمریکایی Charles River Laboratories که امروزه در تمام جهان گسترش پیدا کرده و کیت اندوتوکسین Bioendo از شرکت Xiamen Bioendo Technology Co., Ltd چین هستند.



